

























武漢封城、疫情防控一級響應、疫情數據每日通報、實施疫情聯防聯控工作機制、啟動藥械應急審批通道......自春節前全國打響抗“疫”阻擊戰以來,各級政府與部門便紛紛啟動了各項應急機制,共同筑起了疫情防控的“高墻”。
遠眺大洋彼岸的美國,同樣經過諸多大規模傳染性疾病等公共衛生事件。他們是如何應對重大公衛事件?FDA在其中又扮著演什么樣的角色?他們的舉措對中國抗“疫”有何啟示?日前,美國漢佛萊醫藥顧問有限公司(博濟醫藥子公司)合伙人杜濤博士做客同寫意線上直播間,講述美國應對重大公衛事件的他山之石。
以下為杜濤博士演講實錄整理。

以抗擊甲型H1N1流感為例,首先,FDA為緩解藥品短缺的問題,允許發放已經通過了測試的過期批次的達菲。
其次,通過擴展處方指南,FDA將達菲的使用擴展到1周歲以下的兒童及癥狀持續超過2天的嚴重患者。
再者,FDA還放開了未獲批藥品的使用,例如通過EUA程序,FDA將尚處于臨床研發階段的帕拉米韋靜脈注射液用于治療臨床疾患。
最后,FDA及時地進行信息公開,將所有發布的EUA掛網供公眾閱覽。
他山之石,可以攻玉。
在杜濤博士看來,FDA應對重大公衛事件政策措施對當下新冠病毒疫情來說有如下幾點借鑒:
(1)積極監控供應鏈,聯系醫藥和器械生產廠,確保醫療產品供應鏈的安全;和國際組織密切配合等;
(2)FDA調整了對海外產品合規性稽查和監控策略,如暫停對中國廠商的常規核查和臨檢;
(3)確保消費品安全,和美國海關配合檢疫檢查進口產品;
(4)對診斷、預防和治療疾病的產品研發和使用給予大力支持;
(5)與多方合作,密切檢測疫情進展。
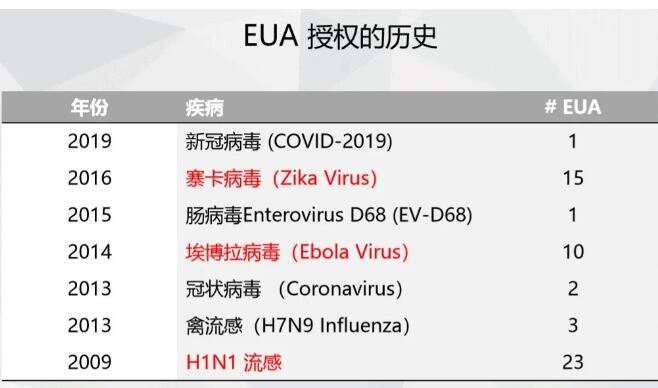
(1)甲型H1N1流感(H1N1-2009)
(2)、埃博拉出血熱(Ebola-2014)
(3)、寨卡病毒病
(4)、新型冠狀病毒(COVID-2019)

