

























 公司新聞
公司新聞


昨天(7月14日),由博濟醫藥主辦、美國漢佛萊承辦的“博濟新藥說”創新藥臨床試驗暨中美雙報巡回沙龍(南京站)在南京城市名人酒店隆重舉行。南京鼓樓醫院機構辦主任李娟,江蘇省人民醫院呼吸科知名專家丁寧博士,博濟醫藥首席科學家、博濟醫藥(北京)公司常務副總經理張學輝博士、首席科學家(細胞與腫瘤方向)孟玉茹博士,副總經理文韶博,博濟醫藥子公司美國漢佛萊首席執行官趙東、法規項目副總裁高翼等近70名來自金陵大地的創新藥專家與領軍人才共襄此次盛會。 會議伊始,文韶博代表主辦方發表致辭。 文韶博在致辭中向與會嘉賓對沙龍的關注與支持表示感謝,希望通過沙龍形式的交流分享增進了解、加深印象、取長補短、攜手共進,共同實現創新藥臨床試驗與中美雙報在南京地區的大發展。 李娟教授以《臨床試驗機構的運行管理》為題展開了演講,正式為這場含金量頗高的學術沙龍拉開了序幕。 李娟在演講中對南京鼓樓醫院臨床機構辦的發展歷程、信息化建設、優勢科室專家、機構辦的各項業務進行了全面的介紹,在她看來,藥物臨床研究機構要緊跟市場發展需求,并通過結合醫院各科室的優勢資源,不斷加強專職化臨床研究隊伍、提高服務質量等方式,助力新藥研發,助力生命健康。 作為江蘇省人民醫院的呼吸科專家,丁寧博士以《自建數據庫進行系列臨床研究》為題,結合自身的發展情況,以睡眠呼吸暫停與心血管疾病的科研與臨床研究成果為例,就科研創新點、 跨學科研究、前瞻性研究、研究設計、資料積累 縱向、橫向拓展、倫理和臨床研究注冊進行了全面解讀,令與會者受益匪淺。 張學輝博士以藥品注冊改革為切入點,援引近年來CDE審評案例,對創新藥、改良型新藥、仿制藥、生物類似藥、中藥新藥等板塊的指導原則和一般要求進行了解讀。他認為,中國加入ICH后,創新藥的審評呈現出逐步與先進監管接軌、大量轉化指導原則、審批尺度逐漸收緊、突出臨床價值等特點,創新藥研發企業需要建立科學、系統、高效的研究體系,滿足創新藥審評審批要求。 孟玉茹博士作為細胞免疫治療與腫瘤領域的知名學者,對相關臨床政策、法規頗為熟稔。在沙龍上,她對《免疫細胞治療產品臨床技術指導原則》的重點內容作了詳細解讀。 “近些年國內細胞和基因治療領域的發展雖如火如荼,但有些品種的IND申報后卻并未獲批臨床。主要是由于藥學研究不符合要求、非臨床研究不完善或安全性風險較大所致。”孟玉茹博士一針見血地指出問題的根源。 在她看來,探索性臨床要考慮給藥間隔,以充分觀察細胞回輸后的不良反應情況。確證性臨床試驗要能充分說明藥物的有效性和安全性,安全性分析集應足夠大。根據產品的性質差異,應進行1-15年的隨訪。 作為近年來的行業熱點,高翼分享的中美雙報專題頗為引人關注。他在演講中介紹了美國FDA IND申報審批的相關流程,并針對于早期項目對接、風險預估、文件收集整理以及Pre-IND會議的有關板塊進行了經驗分享。 整場沙龍一直持續到當晚6時許,沙龍結束后,眾多現場觀眾意猶未盡,紛紛駐足會場,與演講嘉賓深入交流,暢談生物醫藥產業發展大計。 關于博濟醫藥:新藥&醫療器械一站式綜合服務CRO 博濟醫藥科技股份有限公司(簡稱“博濟醫藥”, 股票代碼為300404)創建于2002年,2015年在深圳創業板上市,注冊資本金2.61億元,是一家為國內外醫藥企業提供藥品、醫療器械研發與生產全流程“一站式”外包服務(CRO+CDMO)的新型高新技術企業。公司擁有5.1萬平方米的現代化辦公、實驗和生產場所,目前有超1000名員工,旗下擁有二十多家全資、控股子公司以及十余家關聯業務的參股公司;目前獲得中國醫藥外包公司10強、廣州市科技小巨人企業、廣東省誠信示范企業、廣州市著名商標、中國最具投資價值企業50強、中國醫藥質量管理協會CRO分會會長單位等榮譽稱號;是國內僅有的兩家全流程服務CRO之一,也是以臨床試驗為主要業務的CRO上市公司之一。 博濟醫藥“一站式”服務包括:新藥立項研究和活性篩選、藥學研究(原料、制劑)、藥物評價(藥效學、毒理學)、小分子創新藥一體化服務、臨床研究、中美雙報(注冊服務)、CDMO生產(MAH落地)、技術成果轉化等,涵蓋了新藥研發各個階段。
2022-07-19
2022年7月13日,航天泰心科技有限公司自主研發的HeartCon植入式左心室輔助系統正式獲得國家藥品監督管理局創新產品注冊申請,批準上市(注冊證號:國械注準20223120892)。這將開啟中國心衰治療新時代。博濟醫藥子公司九泰藥械為此項目提供CRO服務。 HeartCon植入式左心室輔助系統為進展期難治性左心衰患者血液循環提供機械支持,用于心臟移植前或恢復心臟功能的過渡治療。對于患有終末期心力衰竭且面臨死亡風險患者的短期輔助、過渡到恢復和過渡到移植的治療將發揮重要作用。 該產品采用泵機一體化設計、磁液懸浮、內流道優化、驅動雙冗余等主要核心技術,均擁有自主知識產權,關鍵技術指標已達到國際同等水平,實現了血泵轉子在血液中的無接觸懸浮運轉。與國內外同類產品相比,具有體積更小質量更輕;無機械軸承,不易產生血栓,無摩擦發熱現象;感染風險低;不受電磁環境的干擾因素影響;產品性能不存在因電器老化導致的隨時間性能下降或故障率上升,可靠性高等優點。航天泰心科技有限公司的研發實力源于其強大的技術背景——中國運載火箭技術研究院。泰達國際心血管病醫院自2009年起與中國運載火箭技術研究院在國內最早開展第三代人工心臟——植入式磁液懸浮心室輔助裝置的研究。2018年,植入式磁液懸浮心室輔助裝置HeartCon獲國家藥品監督管理局批準,進入創新醫療器械特別審批程序。2021年,項目首席專家劉曉程教授率泰達國際心血管病醫院、復旦大學附屬中山醫院、廣東省人民醫院、四川大學華西醫院、天津市第一中心醫院、中南大學湘雅二醫院、福建醫科大學附屬協和醫院、上海長海醫院、鄭州市第七人民醫院、中國醫科大學附屬第一醫院、江蘇省人民醫院11所醫療機構的研究團隊完成“火箭心”注冊臨床試驗。博濟醫藥子公司九泰藥械為此項目提供CRO服務。 人工心臟是最復雜、最精密的醫療器械之一,因產品制造的技術要求高,手術難度大,素有“醫療器械皇冠上的寶石”之稱。過去,該技術一直被美國等發達國家領先和壟斷。中國的人工心臟研究雖然起步晚,但起點高,進展快。劉曉程教授說,泰心醫院和中國運載火箭技術研究院醫工結合潛心研發,取得了詳實的數據和豐富的經驗,相信這顆純國產的“火箭心”將為我國重癥心衰患者及其家庭帶來福音。關于博濟醫藥:新藥&醫療器械一站式綜合服務CRO 博濟醫藥科技股份有限公司(簡稱“博濟醫藥”, 股票代碼為300404)創建于2002年,2015年在深圳創業板上市,注冊資本金2.61億元,是一家為國內外醫藥企業提供藥品、醫療器械研發與生產全流程“一站式”外包服務(CRO+CDMO)的新型高新技術企業。公司擁有5.1萬平方米的現代化辦公、實驗和生產場所,目前有超1000名員工,旗下擁有二十多家全資、控股子公司以及十余家關聯業務的參股公司;目前獲得中國醫藥外包公司10強、廣州市科技小巨人企業、廣東省誠信示范企業、廣州市著名商標、中國最具投資價值企業50強、中國醫藥質量管理協會CRO分會會長單位等榮譽稱號;是國內僅有的兩家全流程服務CRO之一,也是以臨床試驗為主要業務的CRO上市公司之一。 博濟醫藥“一站式”服務包括:新藥立項研究和活性篩選、藥學研究(原料、制劑)、藥物評價(藥效學、毒理學)、小分子創新藥一體化服務、臨床研究、中美雙報(注冊服務)、CDMO生產(MAH落地)、技術成果轉化等,涵蓋了新藥研發各個階段。
2022-07-19
昨天上午(6月28日),廣東藥科大學-博濟醫藥共建研究生聯合培養基地掛牌儀式在博濟醫藥子公司增城僑夢苑分園區博濟生物醫藥科技園(下稱博濟科技園)順利舉行。 廣東藥科大學副校長肖煒、研究生院院長蘇政權、臨床藥學院院長李雄、臨床藥學院黨委書記陳墾、增城經濟技術開發區科技創新局副局長盧靈、創新服務科科長龔奕、增城區委組織部人才工作科科長姜敬非、博濟醫藥董事長王廷春及有關單位相關負責人出席此次活動。(廣東藥科大學副校長肖煒與博濟醫藥董事長王廷春共同為廣東藥科大學-博濟醫藥共建研究生聯合培養基地揭牌) 活動致辭中,王廷春對廣東藥科大學、增城區委區政府各位嘉賓的到來表示歡迎,對廣東藥科大學、增城區委區政府長期以來對博濟科技園發展的關心支持表示感謝。王廷春說,此次廣東藥科大學-博濟醫藥共建研究生培養基地,是雙方在產學研領域合作的又一個里程碑,為雙方搭建了高層次的創新研發平臺。 “期望以此次掛牌儀式為契機,依托政府、高校、企業各自的資源優勢,進一步加深彼此互信,不斷拓展合作空間,構建更多合作形式,共同推進增城區生物醫藥產業發展。” 廣東藥科大學副校長肖煒在講話中介紹了廣東藥科大學的發展歷程與發展成就。在他看來,本次共建研究生聯合培養基地,是校企合作的強強聯合,是產學研合作發展的重要實踐,各自要充分發揮自身優勢,對接各類創新資源,拓展科研合作的深度,攜手共創校企合作發展的新篇章。 隨后,蘇政權、李雄分別就廣東藥科大學的研究生培養和臨床藥學院發展進行了介紹。龔奕則就增城科技發展及僑夢苑建設的相關政策進行了宣講。 在后續的合作交流環節中,盧靈介紹了增城區經濟發展、創新創業發展和科技政策的情況,期望通過政策紅利吸引更多優秀企業到增城發展,促進產學研深度融合,為高校、企業、學生等多方共謀福利。各方就產學研深度融合發展、校企全方位合作、人才培養、人才政策實施、企業建設發展、企業人才需求等問題,深入地交換了意見。 此外,與會嘉賓還赴博濟醫藥總部實驗室參觀,了解了藥物研究中心建設發展狀況和相關藥物研發的進展。博濟醫藥副總經理馬仁強、左聯陪同參觀。 關于博濟醫藥:新藥&醫療器械一站式綜合服務CRO 博濟醫藥科技股份有限公司(簡稱“博濟醫藥”, 股票代碼為300404)創建于2002年,2015年在深圳創業板上市,注冊資本金2.61億元,是一家為國內外醫藥企業提供藥品、醫療器械研發與生產全流程“一站式”外包服務(CRO+CDMO)的新型高新技術企業。公司擁有5.1萬平方米的現代化辦公、實驗和生產場所,目前有超1000名員工,旗下擁有二十多家全資、控股子公司以及十余家關聯業務的參股公司;目前獲得中國醫藥外包公司10強、廣州市科技小巨人企業、廣東省誠信示范企業、廣州市著名商標、中國最具投資價值企業50強、中國醫藥質量管理協會CRO分會會長單位等榮譽稱號;是國內僅有的兩家全流程服務CRO之一,也是以臨床試驗為主要業務的CRO上市公司之一。 博濟醫藥“一站式”服務包括:新藥立項研究和活性篩選、藥學研究(原料、制劑)、藥物評價(藥效學、毒理學)、小分子創新藥一體化服務、臨床研究、中美雙報(注冊服務)、CDMO生產(MAH落地)、技術成果轉化等,涵蓋了新藥研發各個階段。
2022-06-30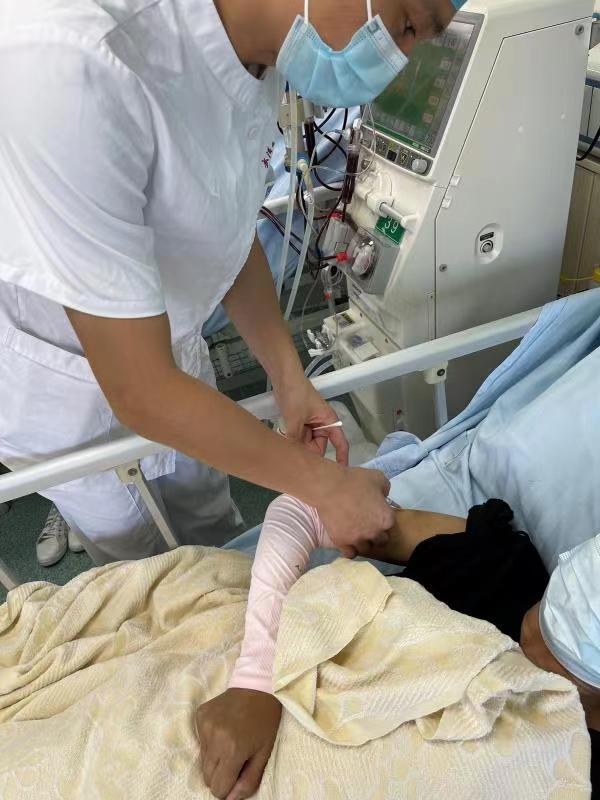
今天(6月15日),rhEPO-FcⅠb/Ⅱ期臨床試驗(下稱rhEPO-Fc項目)首例受試者在武漢大學中南醫院正式入組。 首批受試者入組標志著rhEPO-Fc項目正式進入Ⅰb/Ⅱ期臨床試驗階段。rhEPO-Fc是申辦方自主研發的治療用1類生物制品,博濟醫藥為其Ⅰb/Ⅱ期臨床試驗提供全程CRO服務。 博濟醫藥相關負責人表示,本次入組的首例受試者為腎性貧血患者,受試者入組后將注射rhEPO-Fc項目試驗藥物,并在后續12周內完成多次給藥、檢查等。 “首例受試者入組是本臨床試驗的開始,我們將重點關注受試者在注射rhEPO-Fc項目試驗藥物后在臨床過程中的有效性、安全性和耐受性。”如果試驗順利,后續將陸續啟動多家研究中心,助力rhEPO-FcⅠb/Ⅱ期臨床研究全面提速。 據介紹,rhEPO-Fc項目是一款利用基因治療技術研發治療腎性貧血的新藥,在臨床前研究和前期臨床試驗中展現出了良好的安全性和有效性,具有良好的臨床應用前景,有望成為治療慢性腎臟病透析患者腎性貧血的新選擇。該項目于上周五召開啟動會,3個工作日便完成首例入組。 關于博濟醫藥:新藥&醫療器械一站式綜合服務CRO 博濟醫藥科技股份有限公司(簡稱“博濟醫藥”, 股票代碼為300404)創建于2002年,2015年在深圳創業板上市,注冊資本金2.61億元,是一家為國內外醫藥企業提供藥品、醫療器械研發與生產全流程“一站式”外包服務(CRO+CDMO)的新型高新技術企業。公司擁有5.1萬平方米的現代化辦公、實驗和生產場所,目前有超1000名員工,旗下擁有二十多家全資、控股子公司以及十余家關聯業務的參股公司;目前獲得中國醫藥外包公司10強、廣州市科技小巨人企業、廣東省誠信示范企業、廣州市著名商標、中國最具投資價值企業50強、中國醫藥質量管理協會CRO分會會長單位等榮譽稱號;是國內僅有的兩家全流程服務CRO之一,也是以臨床試驗為主要業務的CRO上市公司之一。 博濟醫藥“一站式”服務包括:新藥立項研究和活性篩選、藥學研究(原料、制劑)、藥物評價(藥效學、毒理學)、小分子創新藥一體化服務、臨床研究、中美雙報(注冊服務)、CDMO生產(MAH落地)、技術成果轉化等,涵蓋了新藥研發各個階段。
2022-06-16
