

























今日(12月20日),國家衛(wèi)健委辦公廳發(fā)布了《新型抗腫瘤藥物臨床應(yīng)用指導(dǎo)原則(2019年版)》(下稱《原則》),該《原則》由“新型抗腫瘤藥物臨床應(yīng)用指導(dǎo)原則”和“各系統(tǒng)腫瘤的藥物臨床應(yīng)用指導(dǎo)原則”兩部分組成,其中“各系統(tǒng)腫瘤的藥物臨床應(yīng)用指導(dǎo)原則”共涉及8類臨床藥物。

新型抗腫瘤藥物臨床應(yīng)用指導(dǎo)原則
(2019年版)



現(xiàn)代抗腫瘤藥物的一個(gè)顯著特征,是出現(xiàn)一批針對(duì)分子異常特征的藥物——即靶向藥物。最具代表性的藥物是針對(duì)表皮生長因子信號(hào)通路異常的酪氨酸激酶抑制劑。目前,根據(jù)是否需要做靶點(diǎn)檢測(cè),可以將常用的小分子靶向藥物和大分子單克隆抗體類藥物分為兩大類(表1)。具體的檢測(cè)靶點(diǎn)詳見各章節(jié)。
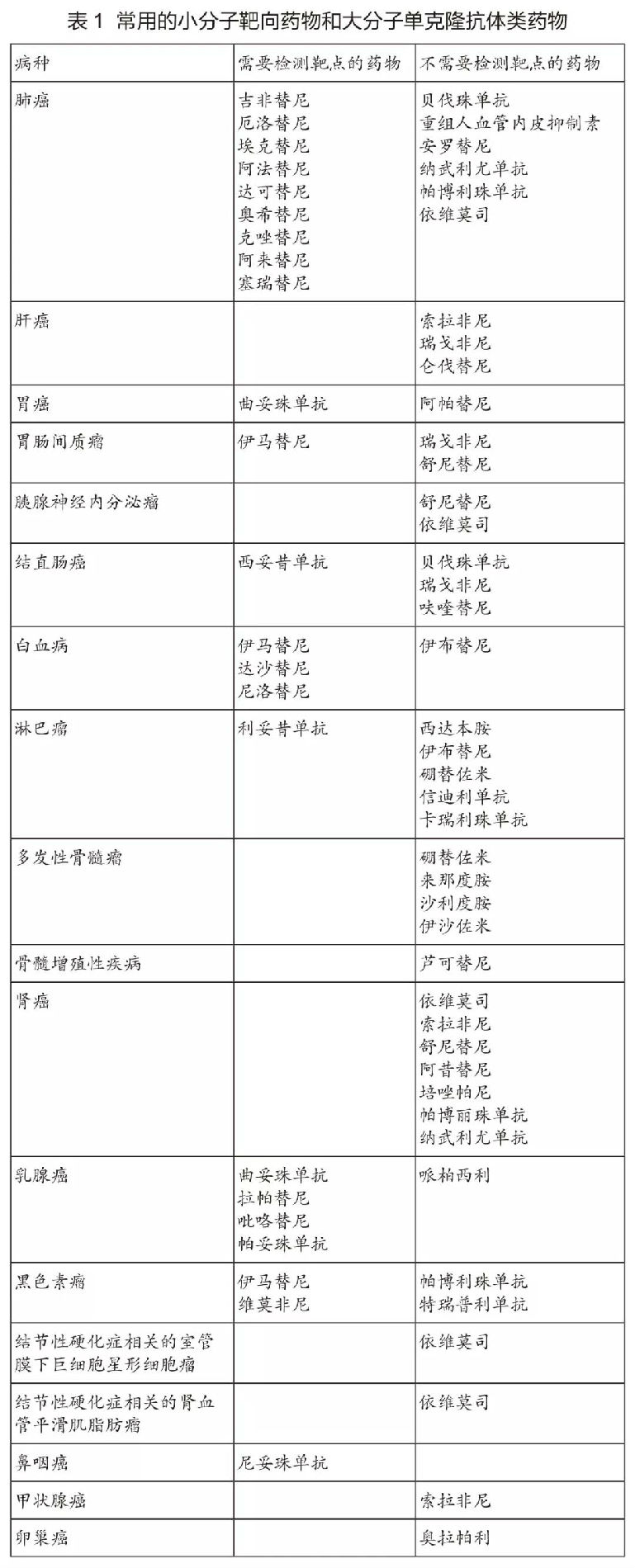
對(duì)于有明確靶點(diǎn)的藥物,須遵循靶點(diǎn)檢測(cè)后方可使用的原則。檢測(cè)所用的儀器設(shè)備、診斷試劑和檢測(cè)方法應(yīng)當(dāng)經(jīng)過國家藥品監(jiān)督管理部門批準(zhǔn),特別是經(jīng)過伴隨診斷驗(yàn)證的方法。不得在未做相關(guān)檢查的情況下盲目用藥。

